
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
BABIOs virustransportsæt opnår FDA 510(k)-godkendelse
BABIOs virustransportsæt opnår FDA 510(k)-godkendelse
Jinan, Kina – oktober 2025— BABIO Biotechnology, en kendt kinesisk producent af medicinske diagnostiske reagenser, annoncerer stolt, at densVirus Transport Kit (Ikke-inaktiverende)har modtagetFDA 510(k) godkendelse (K250205), der officielt validerer dets overholdelse af amerikanske regulatoriske standarder.
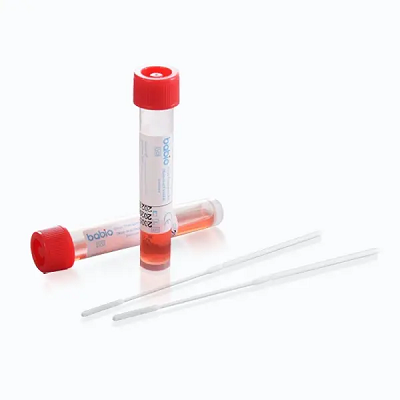
Denne milepæl forstærker BABIOs globale lederskab inden for løsninger til transport af kliniske prøver. Sættet er udviklet til sikker og stabil indsamling af virale prøver, der understøtter downstream-applikationer som f.eksRT-PCR, viral kultur, ogmolekylær diagnostik. Den byder på:
-
✅ Stabilitet ved stuetemperatur
-
✅ Forbedret Hanks løsning med antibiotika
-
✅ DNase/RNase-fri koniske rør
-
✅ Sikker flocking vatpinde med breakpoint design
Sættet fås i flere fyldningsvolumener (1ml-6ml) og pakkestørrelser (20-500 rør), og er ideelt til hospitaler, laboratorier og offentlige sundhedsinstitutioner over hele verden.
Med endaglig produktionskapacitet på 100.000 enheder, BABIO sikrer ensartet udbud og konkurrencedygtige priser. Har tillid tilUSA, Tyskland, og derudover fortsætter BABIO med at levere innovation og pålidelighed i virustransportsystemer. Lær mere på https://www.babiocorp.com.
#VirusTransportKit #FDA510k #BABIO #ClinicalDiagnostics #VTM #RT-PCR #GlobalHealthcare #MedicalDevices #SpecimenCollection


